FALL 3.1 Gewichtsverlust
Ein 37-jähriger Patient sucht den Hausarzt auf, da er seit drei Monaten an übermäßiger Müdigkeit, Leistungsabfall und ungeklärtem Gewichtsverlust von 3 kg leidet. Dem Zahnarzt sind bräunliche Flecke an der Zunge aufgefallen. Der Patient bemerkt eine ungewohnte Bräunung bereits nach kurzdauernder Sonnenexposition.
Klinisch ist der Patient in gutem Allgemeinzustand, Gewicht 72 kg, Größe 176 cm. Kardiopulmonal ist er kompensiert, der Blutdruck beträgt 105/70 mmHg, Puls 70/min regelmäßig. Die Haut zeigt v. a. an den sonnenexponierten Stellen eine vermehrte Pigmentierung, im Stirnbereich findet sich ein hyperpigmentierter Nävus. Die Zunge weist mehrere bräunliche Flecken auf.
3.1.1 Wie lautet Ihre Verdachtsdiagnose?[1]
Lösung 3.1.1
Die Anamnese mit Müdigkeit, Gewichtsverlust und Leistungsintoleranz lässt eine Nebennierenrindeninsuffizienz vermuten. Dazu passen auch die vermehrte Hautpigmentierung sowie die Flecken im Zungenbereich.
3.1.2 Vermuten Sie in diesem Fall eine primäre oder eine sekundäre Nebennierenrindeninsuffizienz?
Lösung 3.1.2
Die Hyperpigmentierung spricht für eine primäre Nebennierenrindeninsuffizienz: Die Schädigung liegt auf Ebene der Nebennierenrinde.
3.1.3 Warum kommt es bei einer primären – im Gegensatz zur sekundären – Nebennierenrindeninsuffizienz zu einer Hyperpigmentierung?
Lösung 3.1.3
Aufgrund des verminderten bzw. fehlenden negativen Feedbacks durch Kortisol wird bei primärer Nebennierenrindeninsuffizienz vermehrt Proopiomelanocortin (POMC) in Hypophyse und Hypothalamus gebildet. POMC ist ein Prohormon, das durch spezifische Proteasen in verschiedene Peptidhormone gespalten wird. Dazu zählen ACTH und unterschiedliche Melanozyten-stimulierende Hormone (MSH). Die MSH bewirken eine verstärkte Hautpigmentierung mit dem typischen olivbräunlichen Hautkolorit. Die Hyperpigmentierung tritt prominent an Stellen mit Lichtexposition oder erhöhter mechanischer Belastung (z. B. Hosenbund) auf, evtl. auch enoral an den Schleimhäuten. Bei sekundärer Nebennierenrindeninsuffizienz liegt die Störung auf Ebene der Hypophyse bzw. des Hypothalamus, die POMC- bzw. MSH-Spiegel sind niedrig.
3.1.4 Welche Laborparameter bestimmen Sie, um Ihre Verdachtsdiagnose zu sichern?
Lösung 3.1.4
Um die Verdachtsdiagnose einer primären Nebenniereninsuffizienz zu sichern, müssen Kortisol basal, ACTH, Na+ und K+ bestimmt werden.
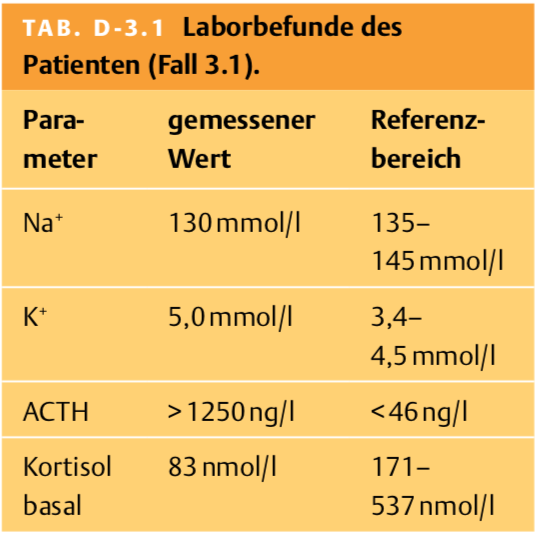
3.1.5 Tab. D-3.1 zeigt die Laborergebnisse des Patienten. Wie interpretieren Sie die Befunde?
Lösung 3.1.5
Das erniedrigte basale Kortisol – zusammen mit dem massiv erhöhten ACTH – ist mit einer primären Nebennierenrindeninsuffizienz vereinbar (fehlendes negatives Feedback). Hyponatriämie und Hyperkaliämie sind Ausdruck eines gleichzeitigen Mineralokortikoidmangels.
3.1.6 Falls keine ACTH-Messung verfügbar ist: Mit welchem Test können Sie in diesem Fall die Nebenniereninsuffizienz beweisen? Erklären Sie das Prinzip!
Lösung 3.1.6
Die Diagnose kann mit dem ACTH-Stimulationstest bewiesen werden, der bei vermuteter Unterfunktion der Hypophysen-Nebennierenachse angewandt wird. Dazu wird i. v. Synacthen® (Tetracosactid) appliziert, ein synthetisch hergestelltesPeptidhormon aus 24 Aminosäuren, die identisch mit den ersten 24 Aminosäuren des ACTH sind. Nach einer bestimmtenZeit wird erneut Kortisol gemessen (peak-Wert). Bei einem Hypokortisolismus wird die Nebenniere durch Synacthen® nicht genügend stimuliert, weil sie zerstört (pri-märe Nebennierenrindeninsuffizienz) oder aufgrund eines ACTH-Mangels (sekundäre Nebennierenrindeninsuffizienz) atrophiert ist. In diesem Fallbeispiel, wo ACTH bereits basal bereits stark erhöht ist, ist kein zusätzlicher Test nötig. Die primäre Nebennierenrindeninsuffizienz ist bewiesen.
3.1.7 Der stimulierte Kortisolwert nach Injektion von 250 μg Synacthen® fällt mit 380 nmol/l deutlich zu tief aus (normal: Anstieg > 550 nmol/l). Die Diagnose “Nebennierenrindeninsuffizienz” ist damit gesichert. Zählen Sie mögliche Ursachen einer primären Nebennierenrindeninsuffizienz auf!
Lösung 3.1.7
Die wichtigsten Ursachen einer primären Nebennierenrindeninsuffizienz sind:
- Autoimmunadrenalitis: autoimmunbedingte Zerstörung der Nebennierenrinde
- Infektionen: z. B. Tuberkulose, HIV, systemische Pilzerkrankungen
- beidseitige Nebennierenmetastasen: z. B. Bronchial- oder Mammakarzinom
- Nebenniereneinblutung: Antikoagulation, Waterhouse-Friderichsen-Syndrom
- infiltrative Erkrankungen: z. B. Amyloidose
- adrenogenitales Syndrom
- Medikamente: z. B. Ketokonazol, Metyrapon, Etomidat
3.1.8 Sie vermuten eine Autoimmunadrenalitis (Morbus Addison). Wie können Sie die Diagnose sichern?
Lösung 3.1.8
Die Diagnose eines Morbus Addison kann durch Bestimmung der Anti-21-Hydroxylase-Antikörper gesichert werden. Diese sind aber nur bei etwa 70 % der Patienten nachweisbar.
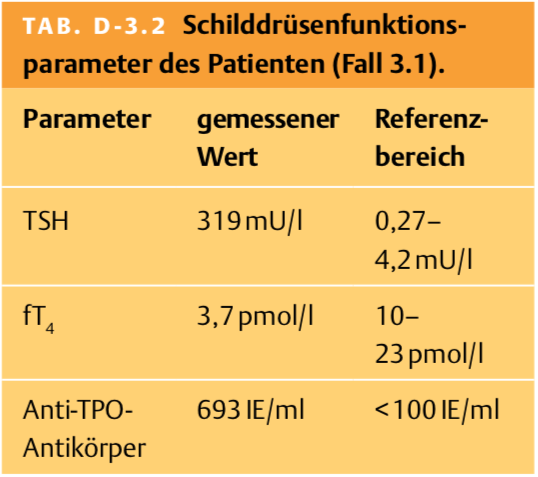
3.1.9 Die Anti-21-Hydroxylase-Antikörper sind deutlich positiv und bestätigen den Verdacht auf eine Autoimmunadrenalitis. Aufgrund der Müdigkeit lassen Sie zusätzlich die Schilddrüsenfunktion des Patienten bestimmen (Tab. D-3.2). Wie interpretieren Sie die Resultate? Gibt es einen Zusammenhang mit dem Morbus Addison?
Lösung 3.1.9
Es liegt eine manifeste primäre Hypothyreose vor. Die Ursache ist eine chronisch-lymphozytäre Thyreoiditis Hashimoto (Anti-TPO-Antikörper positiv). Autoimmunerkrankungen, die endokrine Organe betreffen, treten im Rahmen von polyglandulären Autoimmunsyndromen gehäuft gemeinsam auf.
Weiterer Verlauf
Nach der Diagnose eines polyglandulären Autoimmunsyndroms Typ II wird eine Therapie mit Hydrokortison, Fludrokortison und Levothyroxin eingeleitet. Die Beschwerden bilden sich komplett zurück und die Laborparameter normalisieren sich. Der Patient nimmt wieder 3kg an Gewicht zu. Gut 8 Monate nach Diagnosestellung haben sich die Hyperpigmentierung der Haut und die braunen Flecken auf der Zunge zurückgebildet.
Weitere Informationen: Nebennierenrindenunterfunktion, primären Hypothyreose, polyglanduläre Autoimmunsyndromen
FALL 3.2 Gewichtszunahme
Eine 44-jährige Patientin nimmt innerhalb von zwei Jahren 10kg Gewicht zu. Sie gibt an, weder Ernährung noch körperliche Aktivität signifikant geändert zu haben. Eine Übergewichtsproblematik besteht seit ihren Schwangerschaften, die Patientin hatte nach der letzten Schwangerschaft einen BMI von 29kg/m2. Das Gewicht war lange Zeit stabil, aktuell liegt der BMI bei 32kg/m2. Die Patientin beklagt, dass “vor allem der Bauch wächst”. Im Verlauf entwickelt sie eine arterielle Hypertonie, die mit einem ACE-Hemmer behandelt wird. Außerdem wird eine Dyslipidämie festgestellt und eine Therapie mit einem Statin begonnen. Seit einiger Zeit bemerkt sie vermehrten Durst und muss häufig Wasser lassen. Innerhalb von zwei Monaten kommt es zu drei vaginalen Pilzinfektionen, die eine antimykotische Behandlung erforderlich machen.
3.2.1 Wie ist Ihre erste Beurteilung und Verdachtsdiagnose?
Lösung 3.2.1
Es besteht ein metabolisches Syndrom mit Übergewicht, arterieller Hypertonie und Dyslipidämie. Bei den Symptomen Polydipsie, Polyurie und rezidivierende Mykosen muss an einen Diabetes mellitus gedacht werden.
3.2.2 Sie vermuten einen Diabetes mellitus Typ 2 im Rahmen des metabolischen Syndroms. Wie stellen Sie die Diagnose eines Diabetes mellitus?
Lösung 3.2.2
Die Diagnose “Diabetes mellitus” kann bei einer Nüchternplasmaglukose ≥ 7,0 mmol/l oder einem HbA1c ≥ 6,5 % gestellt werden.
3.2.3 Die Nüchternplasmaglukose der Patientin beträgt 12,3 mmol/l, das HbA1c 9,5 %. Wie würden Sie sie antidiabetisch behandeln?
Lösung 3.2.3
Die wichtigste Maßnahme bei der Diagnose eines Diabetes mellitus Typ 2 ist die Patientenschulung hinsichtlich Ernährung und Lebensstilveränderungen. Zusätzlichwird in dieser Situation als medikamentöse Therapie der Wahl Metformin empfohlen.
3.2.4 Nennen Sie 2 wichtige Kontraindikationen von Metformin! In welchen Situationen sollte Metformin abgesetzt werden?
Lösung 3.2.4
Wichtige Kontraindikationen von Metformin sind Niereninsuffizienz und schwere Herzinsuffizienz, da es bei diesen Erkrankungen eine Laktatazidose auslösen kann. Präoperativ, bei schweren Allgemeinerkrankungen und vor Untersuchungen mit jodhaltigen Kontrastmitteln sollte Metformin immer abgesetzt werden.
3.2.5 Gut 6 Monate später erscheint die Patientin wieder in der Sprechstunde. Sie beklagt nun eine vermehrte Behaarung im Gesichtsbereich, hat erneut 3 kg zugenommen und ist neu amenorrhoisch. Zunehmend macht ihr das Treppensteigen Mühe, sie verspürt dabei eine Kraftlosigkeit in den Oberschenkeln. Die Haut ist dünn geworden und bereits bei geringen Traumata bilden sich Hämatome.
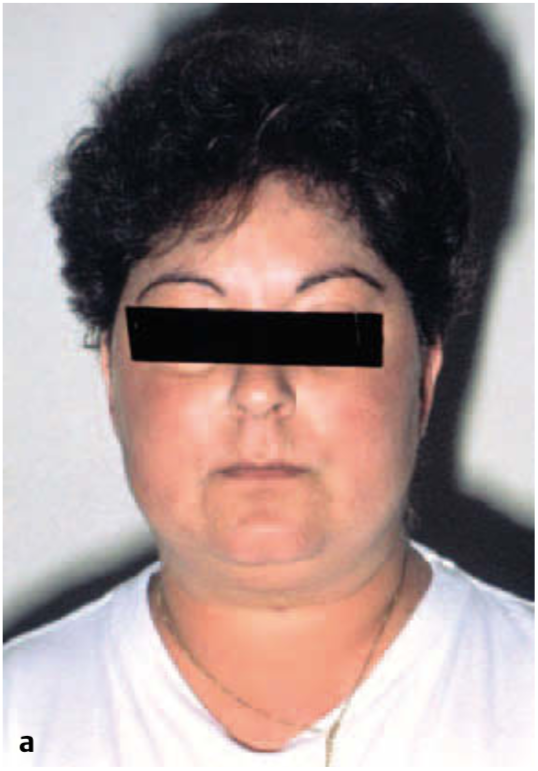
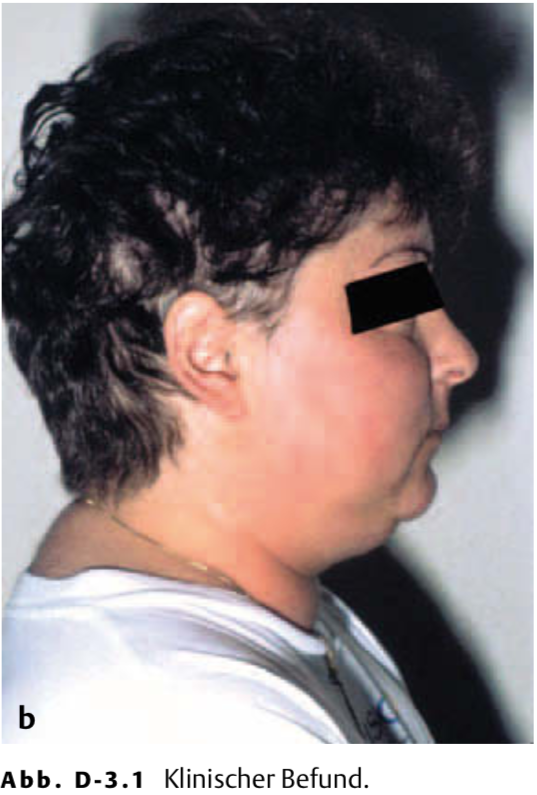
Klinisch: Guter Allgemeinzustand. Größe 168 cm, Gewicht 93 kg, BMI 33 kg/m2. Blutdruck 140/90 mmHg, Puls 80/min regelmäßig. Kardiopulmonal kompensiert. Zentral betonte Fettverteilung, ausgefüllte Supraklavikulärgruben und symmetrische Atrophie der Quadrizeps-Muskulatur, Vollmondgesicht. Generalisierte Hautatrophie mit zahlreichen Suffusionen, Striae rubrae im Abdominalbereich. Hirsutismus im Kinn- und Lippenbereich (Abb. D-3.1).
Wie lautet Ihre Verdachtsdiagnose nun?
Lösung 3.2.5
Die Anamnese und die folgenden klinischen Befunde sind hochverdächtig auf ein Cushing-Syndrom:
- sekundäre Amenorrhö mit Hirsutismus
- typische Hautzeichen: “easy bruising” (Suffusionen und Ekchymosen der Haut nach geringen Traumata), Hautatrophie, Striae rubrae
- zentral betonte Fettverteilung, Voll-mondgesicht, Büffelnacken, ausgefüllte Supraklavikulärgruben
- Muskelatrophie der Oberschenkelmuskulatur
3.2.6 Anamnese und Klinik passen gut zu einem Hyperkortisolismus. Der Diabetes mellitus ist in diesem Fall sekundär aufgrund des Cushing-Syndroms entstanden. Diese Form des Diabetes mellitus wird in die Kategorie der spezifischen Diabetesformen eingeteilt. Welche weiteren Erkrankungen können einen spezifischen Diabetes mellitus zur Folge haben?
Lösung 3.2.6
Weitere spezifische Diabetestypen sind:
- genetische Defekte der β-Zell-Funktion, z. B. MODY
- Erkrankungen des exokrinen Pankreas, z. B. Pankreatitis, Karzinom, zystische Fibrose
- Endokrinopathien, z. B. Akromegalie, Cushing-Syndrom, Glukagonom, Phäochromozytom, Hyperthyreose
- medikamenteninduzierter Diabetes, z. B. durch Glukokortikoide, Nikotinsäure, Schilddrüsenhormone, β-Adrenergika, Thiazide oder Interferon-α
- Infektionen, z. B. kongenitale Röteln, CMV
3.2.7 Mit welchen weiteren Untersuchungen und Tests können Sie den Verdacht des Hyperkortisolismus bestätigen? Beschreiben Sie die Durchführung!
Lösung 3.2.7
Der Verdacht kann mithilfe des Dexamethason-Hemmtests erhärtet werden. Durchführung: Gabe von 1 mg Dexamethason um 23.00 Uhr, Bestimmung des Kortisolwerts am nächsten Tag um 8.00 Uhr. Bei Cushing-Syndrom wird Kortisoldurch Dexamethason nicht supprimiert. Weitere Untersuchungen, die einen Hyperkortisolismus bestätigen:
- erhöhte Ausscheidung von freiem Kortisol im 24-Stunden-Urin
- erhöhtes Kortisol im Speichel um Mitternacht
3.2.8 Das Cushing-Syndrom wird durch einen pathologischen Dexamethason-Hemmtest bestätigt. Die Ausscheidung von freiem Kortisol im 24-Stunden-Urin ist ebenfalls deutlich erhöht.
Sie möchten nun wissen, ob es sich um ein zentrales (ACTH-produzierendes Adenom des Hypophysenvorderlappens = Morbus Cushing) oder ein adrenales Cushing-Syndrom handelt. Welchen Parameter können Sie zur Differenzierung beiziehen?
Lösung 3.2.8
Das zentrale und das adrenale Cushing-Syndrom können durch die Bestimmung von ACTH differenziert werden: Bei der adrenalen Form (z. B. Nebennierenrindenadenom) ist ACTH supprimiert, bei Morbus Cushing normal bis erhöht.
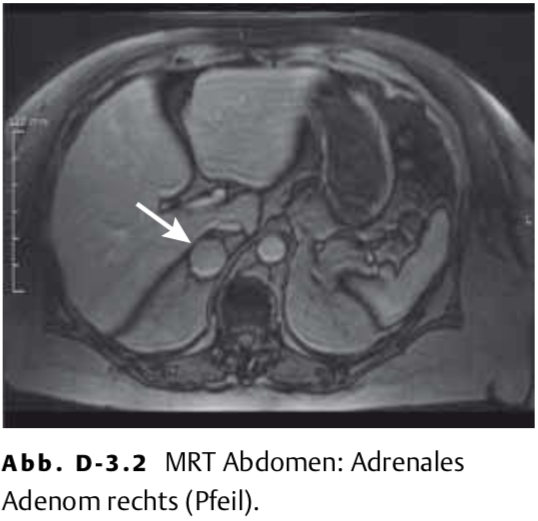
3.2.9 ACTH ist supprimiert, worauf eine MRT des Abdomens durchgeführt wird. Diese zeigt eine 3 cm große Raumforderung der rechten Nebenniere (Abb. D-3.2).
Die Patientin wird in der Folge rechtsseitig adrenalektomiert. Unmittelbar nach der Operation entwickelt sie Symptome einer Nebennierenrindeninsuffizienz (Addisonsymptomatik) mit Hypotonie, Schwäche und Präsynkopen. Was ist die Ursache dieser “Addisonkrise”? Wie hätte sie vermieden werden können?
Lösung 3.2.9
Durch den adrenal bedingten Hyperkortisolismus ist die ACTH-Sekretion – ähnlich wie bei einer langdauernden exogenen Glukokortikoidtherapie – dauerhaft supprimiert. In der Folge atrophiert die nicht betroffene Nebenniere, es kann Monate bis Jahre dauern, bis sich ihre Funktion erholt. Die Patienten werden deshalb routinemäßig nach der Operation mit Hydrocortison substituiert.
Weiterer Verlauf
Der postoperative Verlauf bei der Patientin ist günstig. Innerhalb eines Jahres verliert sie 15kg an Gewicht und der ACE-Hemmer sowie Metformin können gestoppt werden.
Weitere Informationen: Diagnostik des Diabetes mellitus, Diabetes mellitus Typ 2, Diagnostik bei Nebennierenerkrankungen, Hyperkortisolismus
- Falls die Lösungen schon 'geöffnet' und sichtbar sind, benutzen Sie bitte einen anderen Browser (z.Bsp. Firefox oder Chrome). ↵