25.1 – Jodmangelstruma |
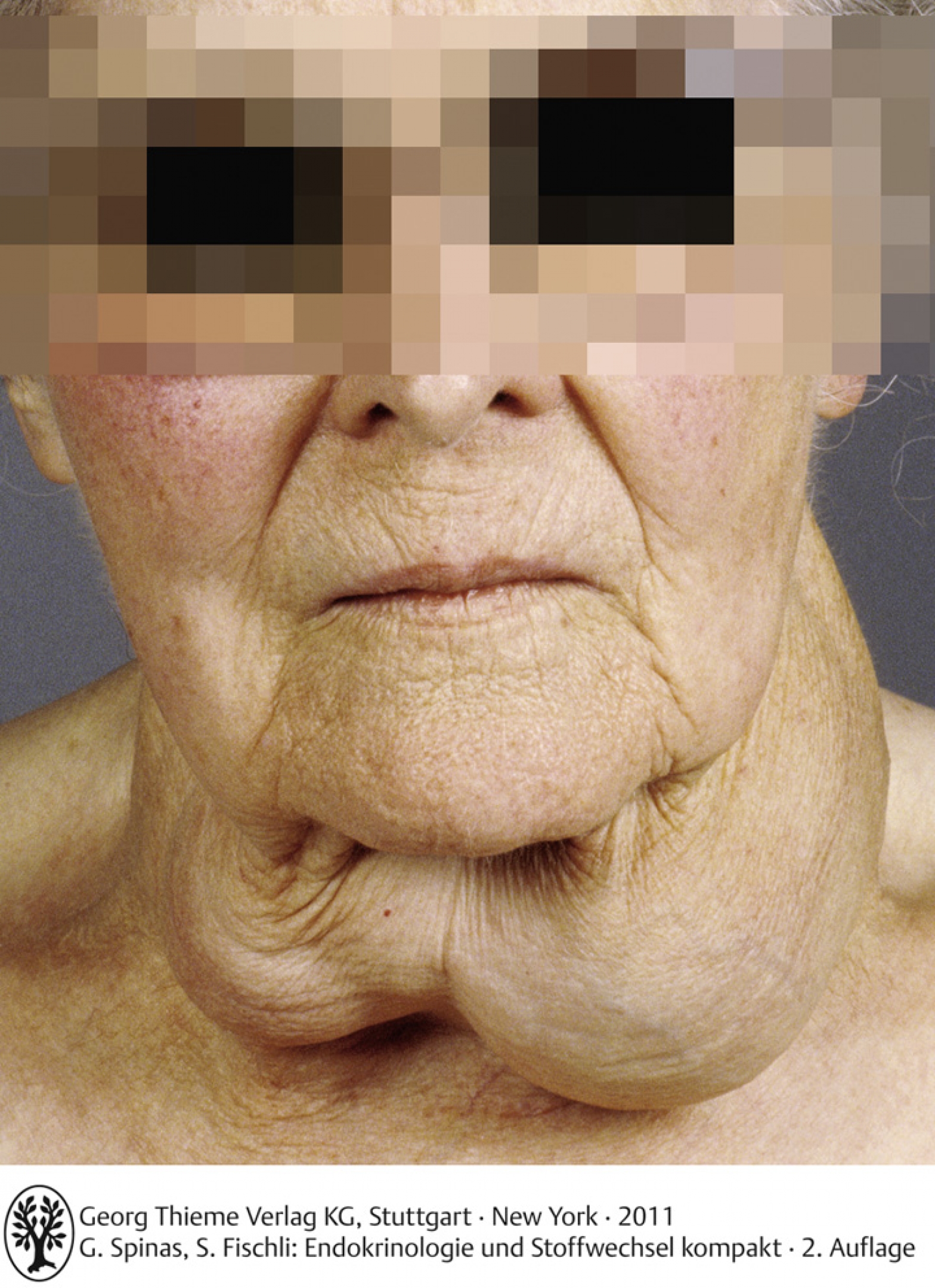
Die Vergrösserung einer Schilddrüse wird als Struma (“Kropf”) bezeichnet.
- gesamte Schilddrüse vergrössert: diffuse Struma
- nur teilweise vergrössert: knotige = adenomatöse Struma
WICHTIG
Jodmangel (zu geringer Gehalt an Jod im Trinkwasser) ist in Mitteleuropa häufigste Ursache für Entstehung einer Struma = endemische Struma.
Bei Jodmangel wird zu wenig T3 und T4 produziert → TSH steigt reaktiv an TSH wirkt wachstumsfördernd → diffuse Struma → knotige Struma.
Kopressionssyndrome (Tracheomalazie, Schluckstörungen, Kompression der Nerven und der Halsgefässe) bei sehr grossen knotigen Strumen.
25.1.1 – Pathogenese
Infolge Jodmangel wird zu wenig T3 und T4 produziert → Rückkoppelungshemmung auf die Hypophyse nimmt ab → Vermehrte Sezernierung von TSH → diffuse Hyperplasie des Schilddrüsengewebes → im Verlauf kommt es auch zu Vernarbungen, Einblutungen und Verkalkungen.
MERKE
Dauernde Wachstumstimulation durch TSH können zu lokalen Mutationen führen.
Entwicklung zu einer TSH-unabhängigen (autonomen) Struma (fokale Autonomie).
25.1.2 – Klinik
Initial diffuse Vergrösserung, dann knotige und asymmetrische Vergrösserung.
Einteilung der Schilddrüsen Vergrösserung nach WHO:
- Grad I : Struma tastbar und sichtbar bei Reklination
- Grad II: sichtbare Struma
- Grad III: sehr grosse, aus Entfernung sichtbare Struma
Kompressionssymptome:
- Tracheomalazie (substernale Ausdehnung der Struma kann zu Kompression und der Trachea führen): Dyspnoe, Stridor und Schluckbeschwerden
- Nervenausfälle: Heiserkeit durch Kompression der N. laryngeus recurrens, Horner Syndrom
- Zeichen der oberen Einflussstauung (gestaute Halsvenen)
MERKE
Rasch wachsende Knoten, ein Hornersyndrom oder eine Rekurrensparese sind malignomverdächtig!
25.1.3 – Diagnostik
- Labor: TSH, fT4, TPO-Ak und TRAK
- Bildgebung: Sonografie , evtl. MRT
- Feinnadelpunktion: Knoten > 10 mm
25.1.4 – Differenzialdiagnosen
Schilddrüsenkarzinom
Struma mit Hyperthyreose: Morbus Basedow, autonomes Schilddrüsenadenom, Anfangsstadium einer Thyreoiditis.
Struma mit Hypothyreose: Hashimoto-Thyreoiditis, Spätstadium von Thyreoiditiden, genetische Defekte der Schilddrüsenhormonsynthese, ektope Schilddrüse (z.B. Zungengrundstruma).
Schilddrüsenhormonresistenz (selten): periphere Hormonresistenz durch Defekt des Schilddrüsenhormonrezeptors → Erhöhung von T4 und T3 bei normalem TSH-Spiegel, meist euthyreote Klinik.
strumigene Substanzen: Lithium, Perchlorat, Meeresalgen (Kelp, stark jodhaltig), Thiozyanate in einigen Kohlarten, Jod in hohen Dosen.
25.1.5 – Therapie
Totale Thyreoidektomie bei grossen Strumen oder grossen Knotenstrumen mit mehreren Knoten.
Absolute Operationsindikation: Kompressionssymptome, therapierefraktäre Hyperthyreose bei grosser Struma und deutlicher Grössenzunahme.
MERKE
Nach totaler Thyreoidektomie oder Radiojodtherapie ist in den meisten Fällen eine lebenslange Substitution mit Thyroxin notwendig.
25.2 – Schilddrüsenüberfunktion |
WICHTIG
Klinisches Syndrom, das durch übermässige Schilddrüsenhormonkonzentrationen im Blut (damit “verstärkte” periphere Wirkung der Schilddrüsenhormone) verursacht wird.
25.2.1 – Ursachen von Hyperthyreose
- Morbus Basedow (Grave’s disease)
- Toxisches (autonomes) Adenom
- Toxische multinoduläre Struma
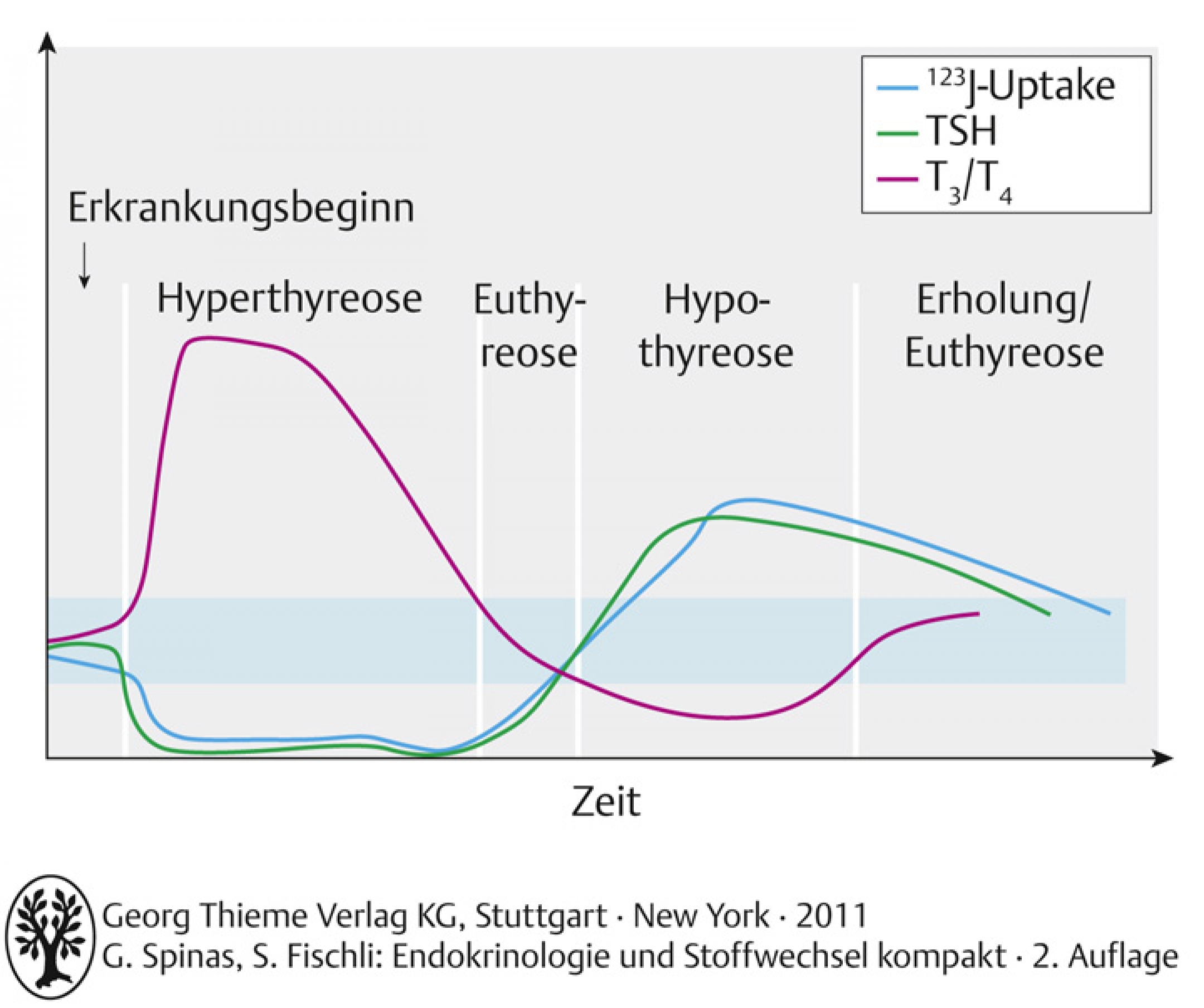
- Hyperthyreote Phase einer subakuten oder chronischen Thyreoiditis
- Seltenere Formen
- TSH-sezernierendes HVL-Adenom (sekundäre Hyperthyreose)
- T3-/T4-Resistenz des HVL
- Metastasierendes Schilddrüsenkarzinom
- Trophoblastenerkrankungen/Keimzelltumore
- Struma ovarii (Teratom mit schilddrüsenhormonproduzierendem Gewebe)
- Thyreotoxicosis factitia
25.2.2 – Morbus Basedow (Graves` Disease)
WICHTIG
Durch stimulierende Autoantikörper gegen TSH Rezeptor (TRAK) induzierte Hyperthyreose.
Manifestiert sich durch eines oder mehrere der folgenden Symptome:
- Hyperthyreose
- Struma
- endokrine Ophthalmopathie (Exophthalmus)
- Dermopathie (prätibiales Myxödem, Akropachie)
Ätiologie und Epidemiologie
- Autoimmunerkrankung mit familiärer Prädisposition
- assoziiert mit HLA-DR3
- assoziiert mit anderen Autoimmunkrankheiten (Diabetes mellitus Typ 1, M. Addison, chronische Polyarthritis)
- Frauen 8x häufiger betroffen als Männer
- Erkrankungshäufigkeit am höchsten zwischen dem 20. und 40. Lebensjahr
Pathogenese und Symptomatik
MERKE
Rauchen verschlechtert Verlauf und Prognose der endokrinen Orbitopathie.
Morbus Basedow und Schwangerschaft
Transplazentarer Übertritt bei hohem TRAK-Titer Hyperthyreose beim Fötus.
Diagnostik
- fT4 ↑, fT3 ↑, TSH supprimiert
- Schilddrüsenautoantikörper: bei M. Basedow sind TRAK typisch (in 30% aber negativ)
- zusätzlich können Anti-TPO-Antikörper vorhanden sein (als Zeichen der autoimmunen Schilddrüsenerkrankung)
- Sonographie: Struma diffus echoarm, inhomogene Binnenstrukturen als Zeichen der Infiltration, Hypervaskularisierung (Douplexsonografie)
- Schilddrüsen-Szintigramm: diffus vergrösserte Struma mit vermehrter Radioiodaufnahme (nur in Ausnahmefällen indiziert, Abb. A-3.11 c)
- bei endokriner Orbitopathie: ophthalmologische Untersuchung mit Perimetrie und ggf MRT der Orbita (Abb. A-3.15)
Therapie
MERKE
Bei Radiojodtherapie können durch Zerstörung des Schilddrüsengewebes viele Antigene frei werden → Stimulation der Immunantwort → Verschlechterung endokrine Orbitopathie
25.2.3 – Schilddrüsenautonomie
WICHTIG
Hypersekretion von T3/T4 durch autonomen (TSH-unabhängigen) Schilddrüsenbezirk
- fokale Autonomie: solitärer Knoten (autonomes Adenom)
- multifokale Autonomie: mehrere Knoten (toxische Knotenstruma)
- diffuse Autonomie
Ätiopathogenese und Epidemiologie
- häufig: aktivierende Punktmutation des G-Proteins des TSH-Rezeptors (im Adenom) → konstitutive Stimulation der Schilddrüsenfunktion (gain-of-function-Mutation)
- prädisponierender Faktor: konstante Stimulation der Schilddrüse durch TSH (z.B. bei Iodmangel-Struma)
- auslösen einer Hyperthyreose durch exogene Jodzufuhr (zB. jodhaltige Kontrastmittelverabreichung oder Amiodarone)
- häufig ältere Patienten ( > 50. LJ)
Klinik
- oligosymptomatisch, gelegentlich palpabler Einzelknoten oder Knotenstruma
MERKE
Ein autonomes Adenom ist oft ein Zufallsbefund bei der Abklärung von Herzrhythmusstörungen, Tachykardien, Gewichtsverlust, Schwächezuständen.
Diagnostik
Laborbefunde:
fT3 ↑, fT4 ↑, TSH supprimiert, keine Antikörper
Sonographie: Knoten, evtl. regressive Veränderungen
Szintigrafie:
- fokale Autonomie: einzelner heisser Knoten, restliches Schilddrüsengewebe supprimiert (Abb. A-3.11 d)
- multifokale Autonomie: mehrere heisse Bezirke, daneben auch kalte Bezirke (Abb. A-3.11 d)
- diffuse Autonomie: verstärkte Radionuklidanreicherung über der gesamten Schilddrüse
MERKE
Bei älteren Patienten mit palpabler oder bekannter Knotenstruma: vor jodhaltiger Kontrastmittelapplikation Schilddrüsenwerte bestimmen!
Auch bei subklinischer Hyperthyreose keine Gabe von jodhaltigem Kontrastmittel wegen Gefahr von hyperthyreoter Entgleisung.
Bei notfallmässigen Untersuchungen: Gabe von Perchlorat vor Kontrastmittelgabe → Jodaufnahme wird blockiert.
Differenzialdiagnose von Morbus Basedow und Schilddrüsenautonomie
| Morbus Basedow | Schilddrüsenautonomie | |
| Alter | v.a. 20.-40. Lebensjahr | v.a. > 50. Lebensjahr |
| anamnestischer Jodmangel | nein | evtl. ja |
| anamnestische Jodexposition1 | meist nein | evtl. ja |
| anderer Autoimmunerkrankungen2 | evtl. ja | nein |
| Klinik | Struma diffusa evtl. endokrine Orbitopathie evtl. Hautzeichen (Myxödem. Onycholyse) |
Schilddrüse normal gross oder multinoduläre Struma |
| TRAK | in 70-80% positiv | negativ |
| Anti-TPO-Ak | häufig positiv | negativ |
| Sonografie | Echoarmut, Inhomogenität, gesteigerte Perfusion (Doppler) | ein oder mehrere Knoten, evtl. regressive Veränderungen |
| Szintigrafie | Diffuse Aktivitätssteigerung über beiden Schilddrüsenlappen | ein oder mehrere “heisse” Bezirke, evtl. Suppression des restlichen Gewebes, evtl. “kalte” Knoten |
1z.B. Kontrastmittelapplikation, Amiodaron
2z.B. Diabetes mellitus Typ 1, Vitiligo, Sprue
Therapie
- Radiojodtherapie bei kleineren Adenomen und älteren Patienten mit hohem OP-Risiko
- chirurgische Resektion bei grösseren Knoten, Struma multinodosa, jüngere Patienten
25.2.4 – Amiodaroninduzierte Hyperthyreose
Pathogenese
- Amiodaron strukturell mit Thyroxin verwandt, enthält 2 Jodatome
- 200mg Amiodaron (normale Einzeldosis): Aufnahme von 6mg anorganisches Jod (20faches der normalen Tagesdosis)
- Jodbelastung kann sowohl Hyper- als auch Hypothyreose auslösen
- Amiodaron hemmt 5`- Dejodinase → hemmt Konversion von T4 zu T3
- Amiodaron kann Follikelzellen direkt schädigen → Thyreoditis
- Amiodaron ist lipophil und verteilt sich im Fettgewebe → lange Eleminationshalbwertszeit von 90 -100 Tagen
2 Typen von amiodaroninduzierter Hyperthyreose:
| Typ I | Typ II | |
| Mechanismus | De-novo Synthese von Schilddrüsenhormonen → jodinduzierte Hyperthyreose |
Thyreoiditis, Freisetzung von Schilddrüsenhormonen durch Gewebezerstörung |
| vorbestehende Thyreopathie | ja: Struma, Autonomie, selten latenter Morbus Basedow | meist keine |
| Jod-Uptake (Szintigraphie)1 | erhöht | vermindert |
| Therapie | Thyreostatika, evtl. Perchlorat, Operationen, Radiojodablation | Glukokortikoide |
Klinik
- oft oligosymptomatisch
- gelegentlich Vorhofflimmern oder Verschlechterung der Herzinsuffizienz
Diagnostik
- fT4 ↑ ↑, fT3 ↑, TSH supprimiert
- Sonographie, Szintigrahie wegen Jodkontamination durch Amiodaron nicht aussagekräftig
Eine Szintigraphie ist wegen der Jodkontamination bzw. der langen Halbwertszeit von Amiodaron häufig nicht aussagekräftig
Therapie
Amiodaroninduzierte Hyperthyreose Typ I: Thyreostatika evtl. in Kombination mit Perchlorat. Bei Therapierefraktären Fällen: Radiojodtherapie oder Thyreoidektomie
Amiodaroninduzierte Hyperthyreose Typ II: Glukokortikoide
häufig Mischformen
evtl. Weiterführung der Therapie mit Amiodaron wegen kardialer Indikation!
MERKE
Amiodaron kann Hyper- und Hypothyreose verursachen.
25.2.5 – Seltene Formen
25.2.6 – Thyreotoxische Krise
WICHTIG
Komplikation der Hyperthyreose mit akuter Exazerbation aller Symptome einer Schilddrüsenüberfunktion (oft lebensbedrohlich).
Ätiopathogenese
Plötzliche Freisetzung von Schilddrüsenhormonen (verminderte Bindung an TBG) und Katecholaminen (Stress) bei Patienten mit hyperthyreoter Stoffwechsellage
mögliche Auslöser:
- Jodexposition bei funktioneller Autonomie
- Stressereignisse bei Patienten mit unerkannter Hyperthyreose: Myokard-Infarkte, Operationen, Unfälle, Sepsis, Verbrennung
- Exazerbation einer bereits bestehenden, schweren Hyperthyreose
- intensive Manipulation am Halsbereich
- Strumektomie bei M. Basedow ohne adäquate vorherige thyreostatische Therapie
Klinik
- Fieber (bis 41°C) mit Schwitzen und Flush
- ZNS-Symptome mit Delirium, Sopor oder Koma
- gastrointestinale Symptome: Nausea, Erbrechen, Durchfall
- kardiale Symptome: Tachykardie, Vorhofflimmern, dekompensierte Herzinsuffizienz bis kardiogener Schock
MERKE
Behandlung eine thyreotosischen Krise auf der Intensivstation!
Therapie
- Thyreostatika (Carbimazol, Thiamazol) hochdosiert: sofortige Blockade der Hormonproduktion
- β – Rezeptoren-Blocker: Verminderung der Sensitivität für Katecholamine
- Plummerung der Schilddrüse: Jod hochdosiert blockiert Freisetzung von Schildddrüsenhormonen
- Glukokortikoide (Prednisolon/Dexamethason): Hemmt Konversion von T4 zu T3
- evtl. Thyreoidektomie
25.3 – Schilddrüsenunterfunktion: Hypothyreose |
WICHTIG
Subklinische Hypothyreose: TSH ↑, fT4 und fT3 im Normbereich, Patient klinisch euthyreot.
Manifeste Hyperthyreose: TSH ↑, fT4 ↓ und fT3 ↓, Patient klinisch hypothyreot.
25.3.1 – Ätiologie
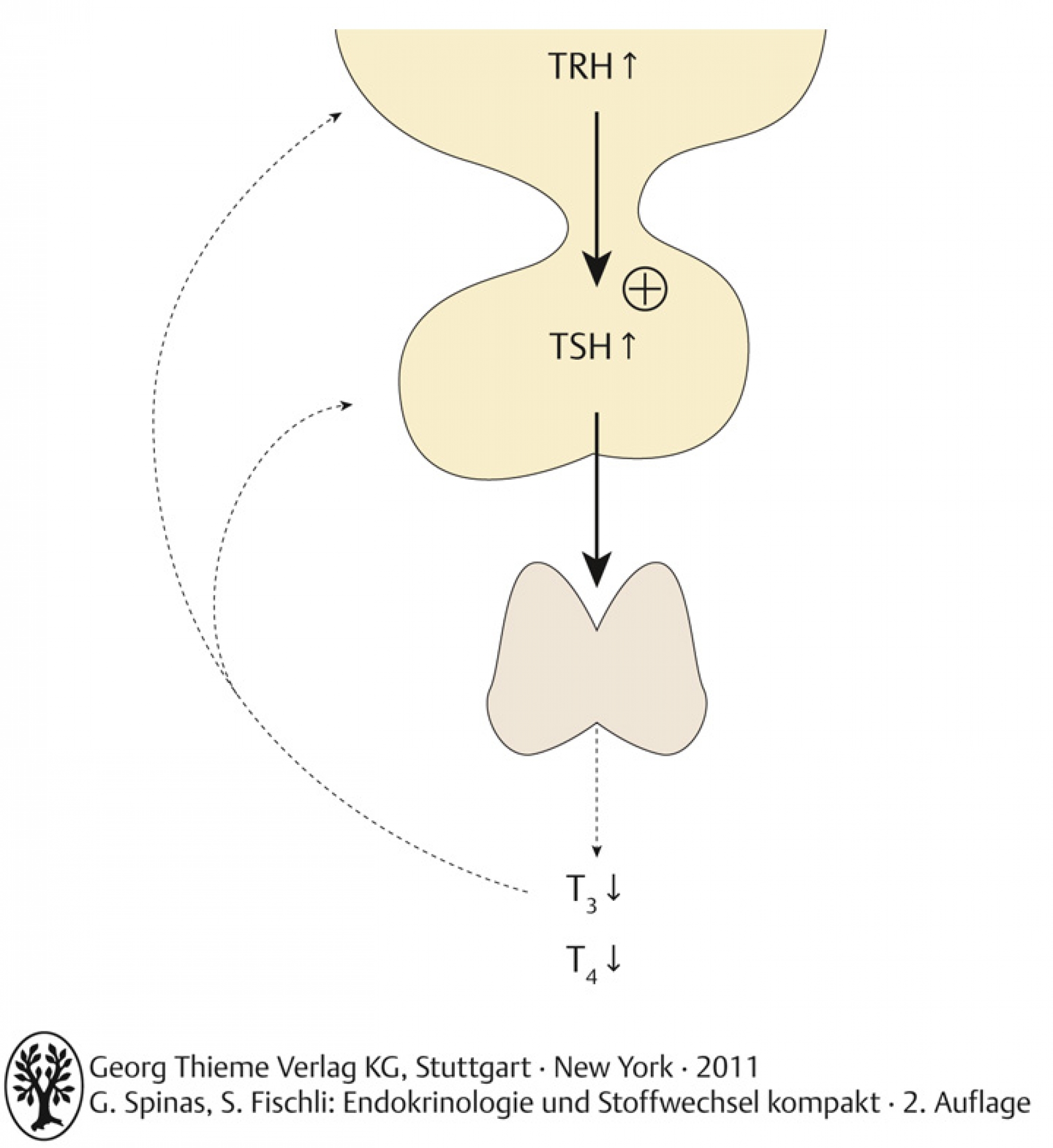
Primäre Hypothyreose
Defekt liegt in der Schilddrüse: TSH ↑, fT3 ↓ und fT4 ↓
- Autoimmunthyreoiditis Hashimoto
- St. n. Strumektomie oder Radiojodtherapie
- St. Radiotherapie im Halsgebiet (z.B. HNO-Tumore, Lymphome)
- nach Jodaufnahme/-applikation (z.B. Amiodaron, Kontrastmittel)
- Jodmangel
- Medikamente: Lithium, Thyreostatika, Amiodaron, Sunitimib
- transient bei Thyreoiditis
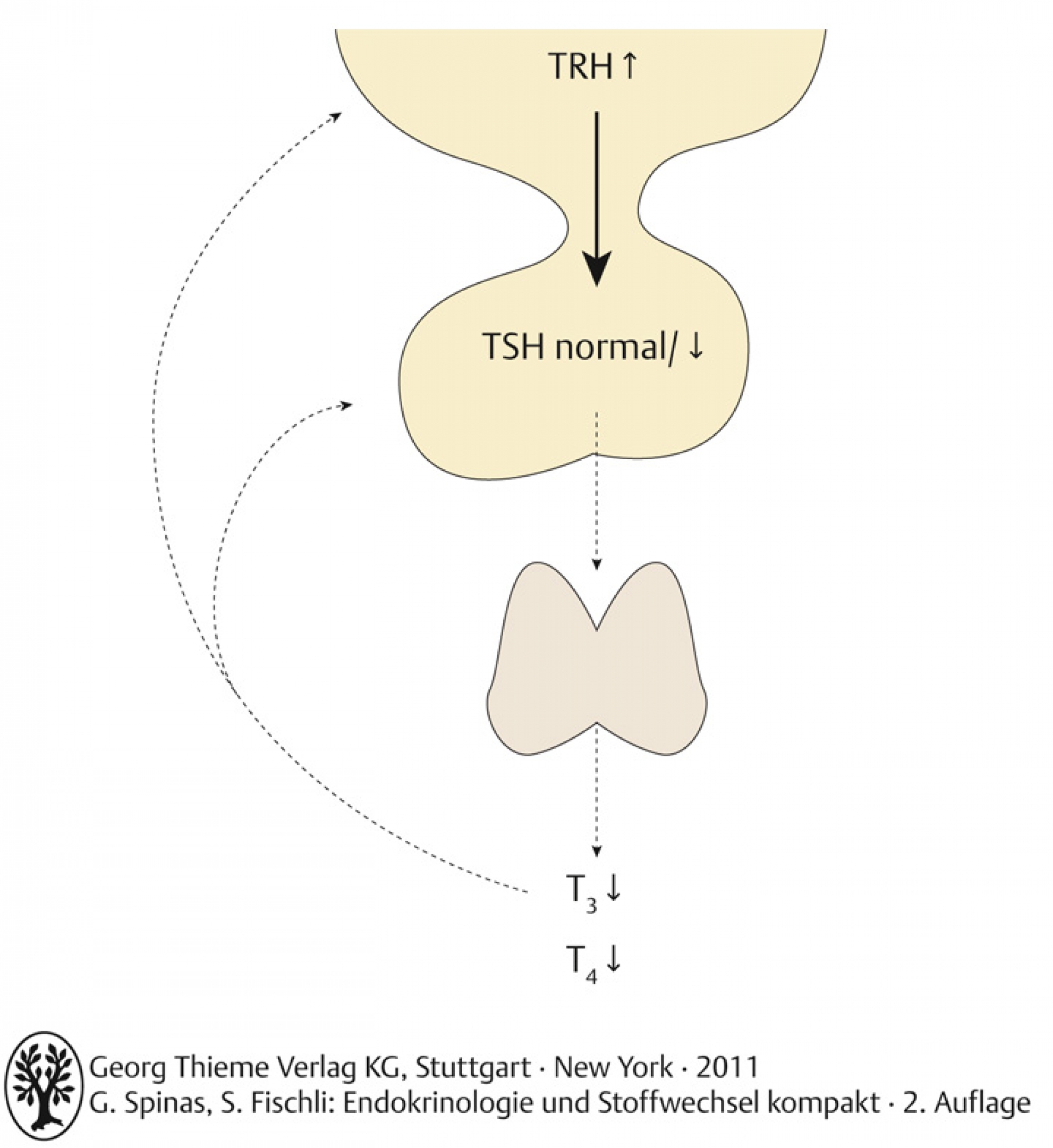
Sekundäre Hypothyreose
Defekt liegt im Hypophysenvorderlappen; TSH ↓ oder inadäquat “normal”, fT3 ↓ und fT4 ↓
- HVL-Adenom, das hormonproduzierendes Gewebe verdrängt
- andere intraselläre Tumoren
- St. n. Hypophysenoperation
- bei Hypophyseninsuffizienz: oft kombiniert mit anderen Hormonausfällen (partielle/totale HVL-Insuffizienz)
25.3.2 – Chronische autoimmune Thyreoiditis Hashimoto
25.3.3 – Hypothyreose des Neugeborenen
MERKE
Frühzeitige Diagnostik und Therapie einer Hyperthyreose im Neugeborenenalter sind essentiel!
Ein verzögerter Therapiebeginn führt zu irreversiblen Schäden der mentalen Entwicklung.
25.3.4 – Hypothyreotes Koma (Myxödema)
WICHTIG
Katecholamine sind wegen verminderter Katecholaminsensitivität des Myokards bei Hypothyreose wirkungslos.
25.4 – Euthyroid Sick Syndrom |
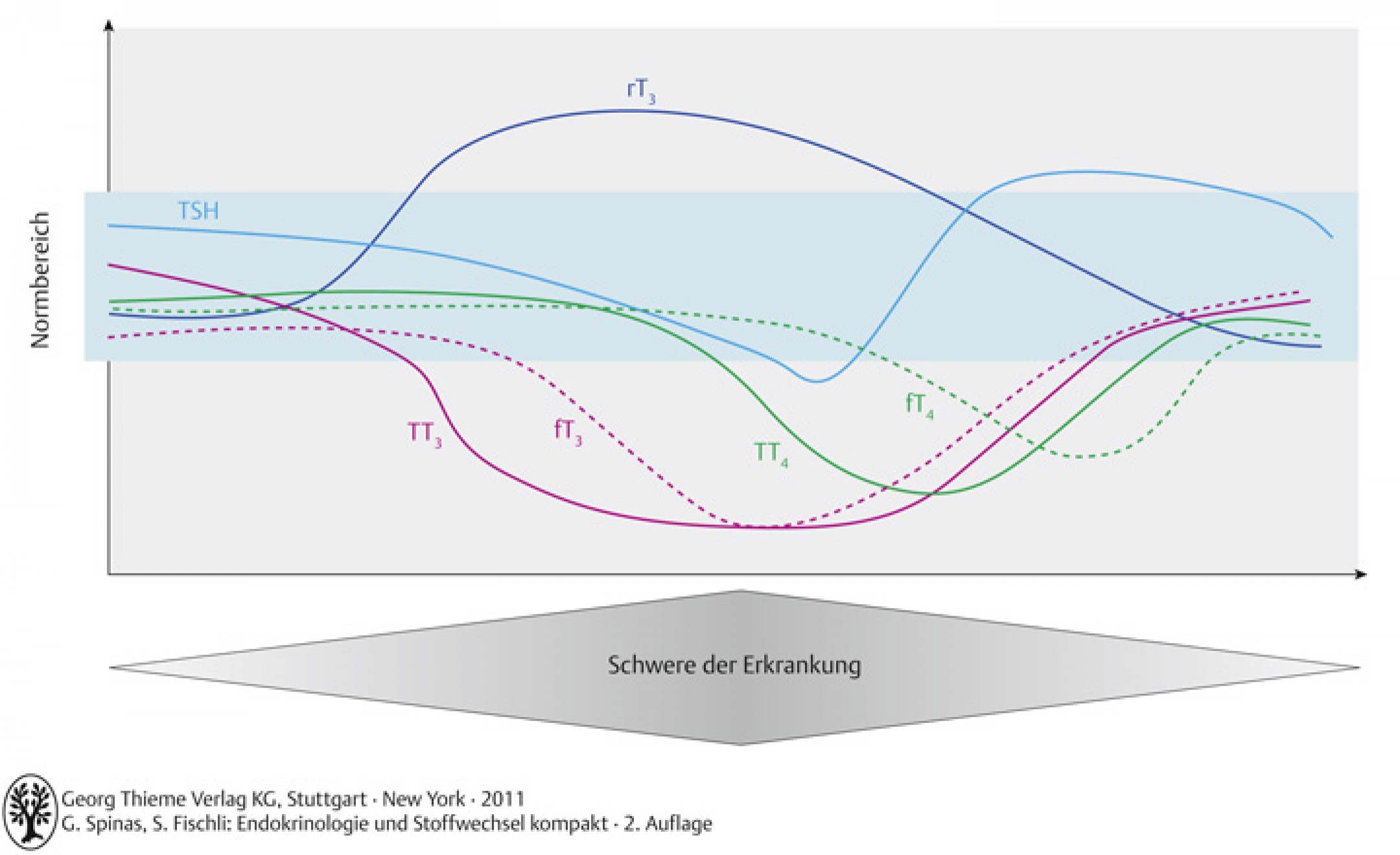
WICHTIG
Akute oder chronische Erkrankungen führen zu einer Verminderung der zirkulierenden T3– und T4-Konzentrationen aufgrund spezifischer Mechanismen (protektive Effekte).
25.4.1 – Ätiopathogenese
Schwere Allgemeinerkrankungen führen zu:
- Veränderungen des peripheren Metabolismus (Dejodinasen): Inhibierung der Typ 1-Dejodinase und Aktivierung der Typ 3-Dejodinase (z.B. durch Zytokine) → verminderte Konversion zu T3 (dafür mehr rT3)
- Veränderung der Bindungsproteine (Abnahme von TBG und Albumin)
- Unterschied zur Hypothyreose: freie Hormonkonzentrationen bleiben normal! (keine Hypothyreose)
Formen des Euthyroid-Sick-Syndrom
| Low-T3-Syndrom | Low-T4 -Syndrom | |
| Ursachen |
|
|
| Laborwerte |
|
|
25.4.2 – Therapie
- Therapie der Grunderkrankung
- keine Verbesserung der Prognose durch Gabe von L-Thyroxin
25.5 – Entzündliche Erkrankungen |
25.5.1 – Subakute Thyreoiditis (Thyreoiditis de Quervain)
25.5.2 – Infektiöse Thyreoiditis
25.5.3 – Fibrosierende Thyreoiditis (Riedel-Thyreoiditis)
25.6 – Schilddrüsenkarzinome
| Art | Häufigkeit | Erkrankungs- alter |
Histologie | Metastasierung | Prognose |
| Papilläres Karzinom | 75-85% | 30.-50. Lj. | oft multifokal
Infiltration der Umgebung hypochrome Nuklei Psammomkörperchen und lamelläre Verkalkungen “follikuläre” Form als Variante (follikärer Aufbau) aber histolog. papilläres Karzinom |
lymphogen regionale Lymphknoten- metastasen in 50 % bei Prognosestellung |
20-Jahresüberleben: -90% |
| Follikuläres Karzinom | 10-20% | 50.-60. Lj. | eingekapselt häufig “mikrofollikuläre” Architektur (DD follikuläres Adenom, Kapsel und Gefässinvasion sichern Dg) |
hämatogen | von Gefässinvasion Fernmetastasierung und Tumorgrösse abhängig |
| Anaplastisches Karzinom | <5% | 60.-80. Lj. | Riesenzellkarzinom, Spindelzellkarzinom, aggressives Wachstum | hämatogen, lymphogen und lokal | schlecht, nicht radiojodsensibel |
| Medulläres Karzinom (neuroendokriner Tumor) |
<5% | 50.-60. Lj. (Ausnahme: fam. Syndrome) |
unilateral, bilateral/multifokal (fam. Syndrome, MEN 2) polygonale Zellen, fibrovaskuläres Stroma, Amyloid, evtl. Zeichen der C- Zell Hyperplasie |
hämatogen und lymphogen | von Grösse und Ursache (sporadisch vs. familiär) abhängig |
25.6.1 – Risikofaktoren
- therapeutische Bestrahlung Hals und Mediastinum
- radioaktive Exposition
- Jodmangel
- genetische Syndrome (z.B. MEN 2)
25.6.2 – Klinik
- derbe mit Umgebung verwachsene Knoten
- schnelles Wachstum
- Zeichen der Umgebungsinfiltration (Horner Sydndrom, Rekurrensparese)
- oft asymptomatscher Zufallsbefund
- evtl. Lymphknotenvergrösserung bei Metastasierung
- Diarrhoe bei medullärem Schilddrüsenkarzinom
25.6.3 – Diagnostik
- Sonographie: echoarm und inhomogen
- Szintigraphie: kalter Knoten
- Feinnadelpunktion: Verifizierung der Diagnose
- Labor: euthyreote Stoffwechsellage, selten Hyperthyreose bei differenzierten follikulärem od. papillärem Karzin; beim medullären Schilddrüsenkarzinom: Kalzitoninspiegel bis 1000x erhöht. CEA: karzinoembrionales Antigen
25.6.4 – Differentialdiagnosen
- Zysten
- Knotenstruma
- fokale Thyreoiditis
- follikuläre Adenome
- Lymphome